Ley de los gases
El estado de un gas depende de la
presión, volumen y la temperatura de tal forma que si una de las variables
cambia el estado del gas también lo hace
porque las dos variables se modifican inevitablemente.
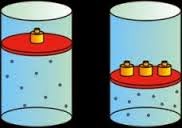
Ley de Boyle
En este caso la temperatura se
mantiene constante, se tiene un proceso isotérmico. Si se aumenta la presión y
el volumen se reduce proporcionalmente, si se duplica la presión el volumen se
reduce a la mitad, o si se reduce la presión a la mitad el volumen del gas se
duplicara. Por lo tanto la presión y el volumen son magnitudes inversamente
proporcionales, razón por la cual el
producto presión-volumen, entonces
presión y volumen si la una sube la otra baja
PV=constante >>>
|
P1V1=P2V2 |
Al graficar presión vs volumen se
obtiene una cuerva característica asi:
La ley
de Boyle se aplica en aquellos procesos en los que la temperatura no varía.


No hay comentarios:
Publicar un comentario